Nel complesso e affascinante universo della biologia cellulare, una recente scoperta sta ridisegnando la nostra comprensione del sistema immunitario e delle sue profonde connessioni con la salute generale dell’organismo. Un team di ricercatori dell’Università di Liegi, in Belgio, ha identificato un “interruttore molecolare” fondamentale, denominato MafB, che agisce come un vero e proprio manuale di istruzioni universale per le cellule immunitarie note come macrofagi. Questo meccanismo, come descritto nello studio pubblicato sulla prestigiosa rivista Immunity, non solo guida queste cellule essenziali nel loro compito di “spazzini” del corpo, ma apre anche orizzonti terapeutici senza precedenti per il trattamento di una vasta gamma di malattie croniche.
I Macofagi: Guardiani Silenziosi della Nostra Salute
Per comprendere l’importanza di questa scoperta, è essenziale soffermarsi sul ruolo dei macrofagi. Queste cellule, presenti in quasi tutti i tessuti del nostro corpo, sono molto più che semplici “mangiatori di cellule” (dal greco “makros”, grande, e “phagein”, mangiare). La loro funzione va ben oltre la fagocitosi di batteri, virus, cellule morte e altri detriti. I macrofagi sono attori poliedrici che contribuiscono attivamente all’omeostasi, ovvero all’equilibrio funzionale, di ogni organo. Si adattano alle esigenze specifiche del tessuto in cui risiedono, pur mantenendo un’identità comune che permette loro di svolgere compiti fondamentali. Fino ad oggi, il meccanismo che consentiva di preservare questa identità condivisa tra tessuti e specie diverse era in gran parte un mistero.
MafB: il Direttore d’Orchestra della Maturazione Cellulare
Lo studio guidato dal professor Thomas Marichal del Laboratorio di Immunofisiologia dell’Università di Liegi ha fatto luce proprio su questo enigma, individuando nel fattore di trascrizione MafB il regolatore genetico centrale. I ricercatori, con Domien Vanneste come primo autore, hanno dimostrato che MafB funziona come un interruttore che attiva o disattiva specifici geni al momento giusto e nel posto giusto. Questo processo è cruciale durante la transizione dei monociti, i precursori immaturi circolanti nel sangue, in macrofagi tissutali a tutti gli effetti.
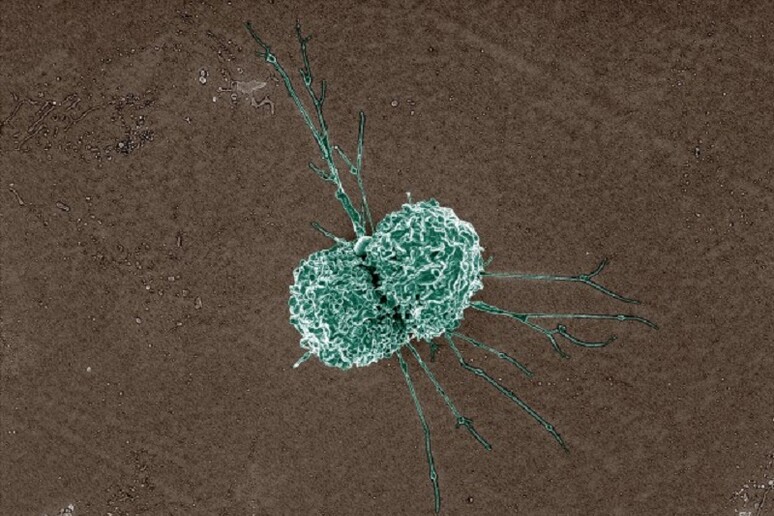
Quando i livelli di MafB aumentano, viene orchestrato un complesso programma genetico che guida la cellula verso la sua piena maturità funzionale. In assenza di MafB, i macrofagi rimangono “bloccati” in uno stato immaturo, incapaci di svolgere correttamente le loro funzioni protettive. Le immagini di microscopia elettronica a scansione prodotte dai ricercatori mostrano chiaramente la differenza: i macrofagi con MafB appaiono maturi e ben formati, mentre quelli che ne sono privi risultano rotondi e sottosviluppati.
“I nostri risultati dimostrano che MafB funziona come un regolatore principale che conferisce ai macrofagi la loro identità e li dota delle capacità necessarie per sostenere la salute degli organi”, ha spiegato l’immunologo Thomas Marichal. “Senza questo programma di istruzioni, queste cellule sono presenti ma non pienamente operative”.
Un Manuale di Istruzioni Universale e le Implicazioni Evolutive
Uno degli aspetti più straordinari emersi dalla ricerca è la conservazione di questo meccanismo genetico nel corso dell’evoluzione. Il ruolo di MafB si è dimostrato essere altamente conservato dai topi agli esseri umani e, più in generale, in tutti i vertebrati. Questa universalità suggerisce che il programma regolato da MafB si sia affermato molto presto nella storia evolutiva perché conferisce un vantaggio adattativo fondamentale: la capacità di avere cellule immunitarie che si adattano alle necessità di organi diversi mantenendo al contempo un’identità funzionale comune.
A livello molecolare, MafB controlla una vasta rete di geni coinvolti in funzioni chiave, tra cui la fagocitosi e il mantenimento dell’equilibrio tissutale. L’analisi epigenetica ha rivelato che MafB regola direttamente geni cruciali per i macrofagi sia nei topi che negli esseri umani, come Csf1r, Mertk, Fcgr1, Cd163 e Zeb2.
Le Conseguenze di un Interruttore “Spento”
Le ripercussioni della mancanza di MafB si estendono ben oltre una semplice risposta immunitaria deficitaria. I ricercatori hanno osservato che l’alterata maturazione dei macrofagi causa difetti a catena in diversi organi. Ad esempio, sono state riscontrate anomalie nel processo di riciclo del ferro che avviene nella milza, così come disfunzioni a livello di polmoni, intestino e reni. Ciò dimostra in modo inequivocabile quanto queste cellule immunitarie siano intrinsecamente legate alla salute dell’intero organismo.
Un macrofago non pienamente funzionale, infatti, non è solo inefficace, ma può diventare un elemento che contribuisce attivamente allo sviluppo di patologie croniche. Molte condizioni, come i disturbi infiammatori, le malattie metaboliche, la fibrosi e le infezioni ricorrenti, vedono i macrofagi disfunzionali giocare un ruolo chiave.
Nuove Frontiere Terapeutiche: Riprogrammare i Guardiani
La scoperta del ruolo di MafB non è solo una pietra miliare per la biologia fondamentale, ma apre prospettive terapeutiche estremamente promettenti. L’idea di poter “riprogrammare” o ripristinare la corretta funzione dei macrofagi agendo su MafB o sulle vie molecolari che esso controlla potrebbe rivoluzionare il trattamento di numerose malattie.
- Malattie infiammatorie croniche: Patologie come l’artrite reumatoide o le malattie infiammatorie intestinali, caratterizzate da un’infiammazione persistente, potrebbero beneficiare di terapie mirate a riequilibrare l’attività dei macrofagi.
- Malattie metaboliche: Condizioni come l’obesità e il diabete di tipo 2 sono associate a uno stato di infiammazione cronica di basso grado (meta-infiammazione), in cui i macrofagi disfunzionali nel tessuto adiposo giocano un ruolo importante. Modulare la loro funzione potrebbe migliorare la sensibilità all’insulina e ridurre le complicanze.
- Riparazione tissutale e fibrosi: I macrofagi sono essenziali anche nei processi di guarigione delle ferite e di rigenerazione dei tessuti. Una loro corretta attivazione potrebbe accelerare la guarigione e prevenire la formazione di tessuto cicatriziale eccessivo (fibrosi) in organi come fegato, polmoni e reni.
In sintesi, questa ricerca identifica MafB come un regolatore centrale e conservato dello sviluppo, dell’identità e della funzione dei macrofagi, gettando nuova luce su come il sistema immunitario protegga in modo sostenibile la salute di più organi. La sfida futura sarà quella di tradurre questa conoscenza fondamentale in strategie cliniche innovative, in grado di riattivare i nostri “guardiani” cellulari e indirizzarli verso la protezione e la guarigione.